Media error: Format(s) not supported or source(s) not found
Descargar archivo: https://f.hubspotusercontent00.net/hubfs/7233254/V%C3%ADdeo%20microbioma%20intestinal%20y%20heridas.mp4?_=2
Al leer el título de este post, os podéis preguntar: ¿Qué relación puede existir entre el intestino y la piel? ¿Qué papel juegan los probióticos en la cicatrización de heridas?
El estudio del microbioma intestinal ha aumentado considerablemente en los últimos años, especialmente por su relación con la respuesta a algunas enfermedades como la diabetes, obesidad, … Recuerdo, hace un año cuando asistí a un seminario sobre microbioma intestinal, donde una investigadora comentaba que existía una relación entre el microbioma intestinal y el momento del enamoramiento, y sus argumentos tenían mucho peso. En ese mismo momento, me pregunté: ¿existirá alguna relación entre el microbioma intestinal y la piel? Así, que me puse a buscar y leer estudios relacionados con este tema.
Empecemos por el principio, la piel, al igual que otras partes del cuerpo, posee una microbiota propia que consta principalmente de cuatro familias (Acinetobacteria, Firmicutes, Proteobacterias y Bacteroidetes). Su función es la de prevenir la invasión de patógenos. La alteración de la microbiota de la piel aumenta el riesgo de presentar infecciones en las heridas, lo que dificultaría su cicatrización. Esto suele pasar en algunas heridas, como las úlceras arteriales o venosas, las úlceras del pie diabético, … Estas infecciones suelen estar causadas, con mayor frecuencia, por bacterias formadoras de biopelículas (Staphylococcus aureus,Pseudomonas aeruginosa, Enterococcus faecalis, Acinetobacter baumannii, Escherichia coli, Klebsiella pneumoniae, Enterobacter spp., Peptostreptococcus spp.). Además, la piel tiene su propio sistema inmunológico, representado por queratinocitos, que pueden participar en funciones inmunes innatas. Esta parte del sistema inmunológico de la piel está en estrecha interacción con su microbiota. Al mismo tiempo, las especies bacterianas de la piel pueden actuar de forma sinérgica con el huésped para erradicar otras especies. Además, los metabolitos de las bacterias pueden influir en el huésped para resolver la inflamación o modular su respuesta inmunitaria básica. En un estudio realizado por Park y cols en 2019, concluyeron que la modulación del microbioma cutáneo puede aplicarse para prevenir o manejar la herida del pie diabético.
Pero, ¿cómo se relaciona la microbiota cutánea con la microbiota intestinal?
La relación entre microbiota intestinal y piel se ha estudiado en diferentes investigaciones, y los resultados muestran la relación entre enfermedades inflamatorias de la piel (dermatitis seborreica, acné vulgar, psoriasis, …), alteraciones en la función e integridad de la piel y un microbioma intestinal alterado. La microbiota intestinal contribuye a la restauración del microbioma de la piel mediante efectos en la inmunidad innata y adaptativa. Estas conclusiones dieron lugar al concepto de eje intestino-piel (figura 1) y cómo las bacterias intestinales pueden tener un impacto positivo en la respuesta a la función de barrera cutánea alterada e inflamación de la piel.

Figura 1. Eje intestino-piel.
Entonces, ¿Cómo podríamos actuar sobre el intestino para mejorar el estado de la piel?
Los patrones dietéticos en nuestra sociedad se han modificado, aumentando la ingesta de grasas e hidratos de carbono y reduciendo la ingesta de fibra. Estas modificaciones han dado lugar a una alteración del microbioma intestinal, lo que contribuye a un estado inflamatorio de nuestro organismo y un aumento en el riesgo de presentar alteraciones cutáneas.
Los probióticos son microorganismos vivos que presentan beneficios en la promoción de la salud, cuando se consumen en una cantidad adecuada. Pueden ayudar a mantener o restablecer el equilibrio del microbioma intestinal y, en consecuencia, mejorar la respuesta del sistema inmune contra la agresión al organismo humano. El consumo de probióticos puede ayudar en la cicatrización de la piel, al estimular la producción de células inmunes, y por sus efectos antagonistas a través de la exclusión competitiva con otros patógenos (figura 2). La Organización para la Cooperación y el Desarrollo Económico (OCDE) afirma que los probióticos son una terapia alternativa al uso tópico de antibióticos debido a la creciente incidencia y transmisión de microorganismos resistentes a los antibióticos.
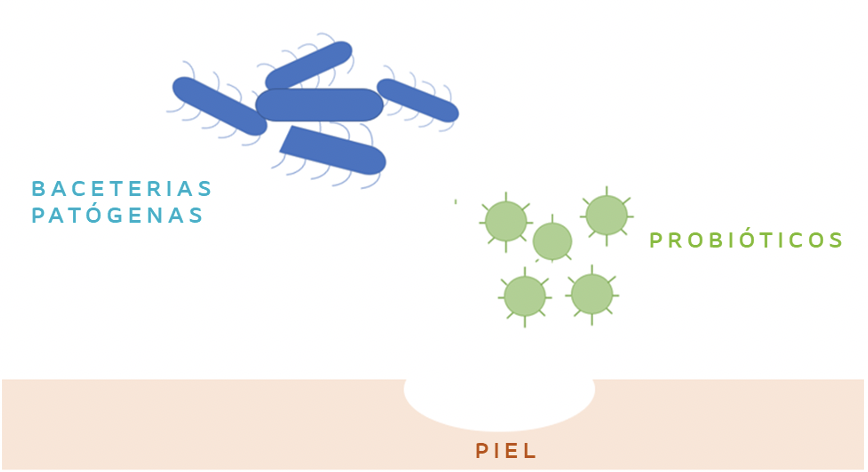
Figura 2. Efecto antagonista de los probióticos
Existen diferentes ensayos clínicos que demuestran la eficacia de los probióticos orales para diversos problemas de la piel. En la investigación realizada por Poutahidis y cols en 2013 observaron que los ratones experimentaron una cicatrización acelerada de heridas después del consumo de Lacotbacillus reuteri. En un estudio realizado en residentes en centros de cuidados a largo plazo, el uso de Lactobacillus paracasei dio lugar a un cambio transitorio en el microbioma de la piel inguinal que, a su vez, redujo la colonización por bacterias Gram-negativas resistentes a múltiples fármacos, lo que reduciría el riesgo de infección.
Alimentos probióticos naturales
- Yogurt.
- Leches fermentadas.
- Miso.
- Tempeh.
- Chucrut.
- Kéfir.
- Kimchi.
- Microalgas.
Conclusiones
Los probióticos orales podrían ser una modalidad simple, segura y barata en el manejo terapéutico de las heridas. Además, los beneficios que aporta en otras patologías (diabetes, obesidad, …), puede mejorar de forma indirecta la cicatrización de las heridas, sin especificación en un tipo de heridas en particular. Se debe seguir investigando en este campo, con el objetivo de obtener evidencias científicas que ayuden a implantar el uso de probióticos en la práctica clínica.
Os remito a la próxima entrada donde se abordará el tema sobre alimentos funcionales y transgénicos y su relación con las heridas.
Bibliografía
Bai Y, Wang Y, Zheng H, Tan F, Yuan C. Correlation Between Facial Skin Microbiota and Skin Barriers in a Chinese Female Population with Sensitive Skin. Infect Drug Resist. 2021; 14: 219-226. doi:10.2147/IDR.S287844.
Callewaert C, Knödlseder N, Karoglan A, Güell M, Paetzold B. Skin microbiome transplantation and manipulation: Current state of the art. Comput Struct Biotechnol J. 2021; 19: 624-631. doi:10.1016/j.csbj.2021.01.001.
Chen G, Chen ZM, Fan XY, et al. Gut-Brain-Skin Axis in Psoriasis: A Review. Dermatol Ther (Heidelb). 2021; 11(1): 25-38. doi:10.1007/s13555-020-00466-9.
Fijan S, Frauwallner A, Langerholc T, et al. Efficacy of Using Probiotics with Antagonistic Activity against Pathogens of Wound Infections: An Integrative Review of Literature. Biomed Res Int. 2019; 2019: 7585486. doi:10.1155/2019/7585486.
Liu-Walsh F, Tierney NK, Hauschild J, et al. Prebiotic Colloidal Oat Supports the Growth of Cutaneous Commensal Bacteria Including S. epidermidis and Enhances the Production of Lactic Acid. Clin Cosmet Investig Dermatol. 2021; 14: 73-82. doi:10.2147/CCID.S253386.
Loomis KH, Wu SK, Ernlund A, et al. A mixed community of skin microbiome representatives influences cutaneous processes more than individual members. Microbiome. 2021; 9(1): 22. doi:10.1186/s40168-020-00963-1
Park JU, Oh B, Lee JP, Choi MH, Lee MJ, Kim BS. Influence of Microbiota on Diabetic Foot Wound in Comparison with Adjacent Normal Skin Based on the Clinical Features. Biomed Res Int. 2019; 2019: 7459236. doi:10.1155/2019/7459236.
Poutahidis T, Kleinewietfeld M, Smillie C, et al. Microbial reprogramming inhibits Western diet-associated obesity. PLoS One. 2013; 8 (7): e68596. doi:10.1371/journal.pone.0068596
Salem I, Ramser A, Isham N, Ghannoum MA. The Gut Microbiome as a Major Regulator of the Gut-Skin Axis. Front Microbiol. 2018; 9: 1459. doi:10.3389/fmicb.2018.01459.
Szántó M, Dózsa A, Antal D, Szabó K, Kemény L, Bai P. Targeting the gut-skin axis-Probiotics as new tools for skin disorder management?. Exp Dermatol. 2019; 28 (11): 1210-1218. doi:10.1111/exd.14016.
Tsai WH, Chou CH, Chiang YJ, Lin CG, Lee CH. Regulatory effects of Lactobacillus plantarum-GMNL6 on human skin health by improving skin microbiome. Int J Med Sci. 2021; 18 (5): 1114-1120. doi:10.7150/ijms.51545.
Wang X, Li Y, Wu L, et al. Dysregulation of the gut-brain-skin axis and key overlapping inflammatory and immune mechanisms of psoriasis and depression. Biomed Pharmacother. 2021; 137: 111065. doi:10.1016/j.biopha.2020.111065.
Zollner-Schwetz I, Scarpatetti M, Pichler G, et al. Effect of a Multispecies Probiotic on Intestinal and Skin Colonization by Multidrug-Resistant Gram-Negative Bacteria in Patients in a Long-Term Care Facility: A Pilot Study. Nutrients. 2020; 12 (6): 1586. doi:10.3390/nu12061586




 (2 votos, promedio: 3,50 de 5)
(2 votos, promedio: 3,50 de 5)





